Une leçon sous ce nom peut avoir lieu en 7e année. Avant d'étudier la chimie, les étudiants seront intéressés de savoir ce qu'étudie la chimie, ce qu'ils font dans les cours de chimie. Le cours est dispensé par des lycéens (quatre élèves chimistes). Avant le début de la dédicace, la salle de chimie est décorée de journaux muraux, de maquettes et de verrerie chimique. Des expériences divertissantes sont présentées, ce qui contribue à l'émergence d'un intérêt pour la chimie.
Cible. De manière ludique, donnez aux enfants une idée de la science de la chimie, des transformations chimiques, de l'importance de la chimie dans la vie humaine.
PENDANT LES COURS
CHIMISTES (tous ensemble). Bonjour!
1er CHIMISTE. Nous sommes des chimistes ! Et la chimie signifie des nuits blanches.
3ème CHIMISTE. Ce sont des laboratoires de chimie.
4ème CHIMISTE. Ce sont des parents qui disent : « Et notre enfant est chimiste.
TOUS. Et c'est la vie !
1er CHIMISTE. Mais vous vous demandez peut-être : pourquoi tout le monde ne devient-il pas chimiste ? Oui, parce que la chimie c'est des nuits blanches.
2ème CHIMISTE. C'est un centième de discours sur la chimie.
3e CHIMISTE (dit en se tenant le nez). Ce sont des laboratoires de chimie.
4ème CHIMISTE. Ce sont les parents qui disent : « Et notre enfant (pouah !) est chimiste ».
TOUS. Et c'est la vie !
1er CHIMISTE (fièrement). Mais nous sommes quand même des chimistes, car la chimie, c'est des nuits blanches !
2ème CHIMISTE. On parle constamment de chimie.
3ème CHIMISTE. Ce sont des laboratoires de chimie !
4ème CHIMISTE. Ce sont des parents qui disent : "Et notre enfant (il se bat la poitrine et dit fièrement) est chimiste !"
TOUS. Et c'est la vie !
1er CHIMISTE. Combien de livres et de contes de fées avons-nous lus dans lesquels de bonnes fées et de puissants sorciers accomplissent des miracles incroyables !
2ème CHIMISTE. Mais ensuite nous avons lu le conte jusqu'au bout, fermé le livre, et au même moment, comme dans un brouillard, les sorciers ont disparu, et il ne restait qu'un vague souvenir de miracles.
3e chimiste. Oui, et comment d'autre ? Après tout, dans la vie, personne n'a encore rencontré de sorciers, parcouru les rues avec eux, n'a pas parlé.
4ème CHIMISTE. Mais cela signifie-t-il que les miracles ne se produisent pas dans la vie ? En aucun cas ! Les gens font des miracles eux-mêmes. Mais ils s'y habituent tellement qu'ils ne voient plus rien de merveilleux. La science est la vraie sorcière de nos jours.
1er CHIMISTE. Et si nous parlons de miracles, alors parmi toutes les autres sciences, la chimie se distingue particulièrement. Pas étonnant qu'elle soit qualifiée de bonne sorcière.
2ème CHIMISTE. Il permet à une personne d'extraire des métaux à partir de minerais et de minéraux, d'extraire des substances de matières premières naturelles, l'une plus merveilleuse et étonnante que l'autre. Il donne naissance à des centaines de milliers de substances, même introuvables dans la nature, aux propriétés utiles et importantes.
3ème CHIMISTE. Il transforme le pétrole en caoutchouc et en essence, le gaz en tissu, le charbon en parfums, colorants et substances médicinales. La liste des bonnes actions que la chimie accomplit est vraiment inépuisable. La chimie nous nourrit, vêtements et chaussures.
4ème CHIMISTE. Chaque personne, sans le savoir, réalise quotidiennement des réactions chimiques, sans même sortir de chez elle : se savonner les mains, allumer des allumettes et du gaz, préparer la nourriture. Oui, et le corps humain lui-même est une grande usine chimique dans laquelle de nombreux réactions chimiques.
1er CHIMISTE.
Eh bien, bien sûr, sans aucun doute,
Faut apprendre la chimie
Sans connaissance de tous les phénomènes
Il est impossible de vivre aujourd'hui.
2ème CHIMISTE.
Faut faire mieux
Nous, amis, dans l'enseignement
Et tu ne devrais pas soupirer
Cette chimie est une torture !
3ème CHIMISTE.
Si vous ne connaissiez pas la chimie
Nous piétinerions toujours à pied :
Bus sans carburant
N'ira jamais!
4ème CHIMISTE.
Pour qu'on grandisse normalement
Fort et fort
Libérations de vitamines
Aussi notre chimie!
1er CHIMISTE.
Pour que les plantes ont poussé,
Des substances ont été inventées.
Ce serait bien pour nous comme ça -
Les grands grandiraient vite.
2ème CHIMISTE.
Le caoutchouc est rare dans la nature
Vous ne pouvez pas vivre sans elle.
Nous marcherions dans les flaques
En bottes de feutre et sans galoches.
3ème CHIMISTE.
Largement entré dans notre vie
Divers plastiques.
En très peu de temps
Ils ont été acceptés par les masses !
4ème CHIMISTE.
Laissez le polymère pour les cheveux
stimuler la croissance,
Inventez vite
Ensuite, les tresses vont pousser.
1er CHIMISTE. Aujourd'hui, c'est votre première introduction à la chimie. Nous allons te montrer quelques trucs que tu pourras bientôt faire en tant qu'étudiant en chimie.
Expérience de démonstration
"Paysage martien"
Sur l'affiche, écrivez à l'avance avec une solution alcoolique de phénolphtaléine: «La chimie est un pays magique», puis, lors de la présentation de l'expérience, essuyez l'inscription incolore avec un tampon imbibé d'alcali. L'inscription deviendra violette.
2ème CHIMISTE. Oui, en effet, la chimie est un pays magique. Après tout, vous ne verrez de tels miracles nulle part ailleurs.
Expérience de démonstration
"Allumer un feu sans allumettes"
Pour l'expérience, préparer une bouillie de KMnO 4 et H 2 SO 4 (conc.). Trempez une tige de verre dans cette bouillie et touchez-la à un coton imbibé d'alcool. Une réaction se produit avec dégagement d'une grande quantité de chaleur et dégagement d'oxygène :
3H 2 SO 4 (conc.) + 2KMnO 4 \u003d K 2 SO 4 + 2MnSO 4 + 5 [O] + 3H 2 O.
L'alcool est inflammable.
3ème CHIMISTE. Au milieu du siècle, il y avait des gens qui passaient beaucoup de temps dans de petits laboratoires, étudiant diverses substances. C'étaient les alchimistes. Les alchimistes ont essayé de transformer les métaux en or. Les rois et les rois gardaient des alchimistes dans leurs palais pour obtenir de l'or pour eux.
4ème CHIMISTE. Mais les alchimistes n'ont pas réussi à transformer les métaux en or, l'alchimie a donc été interdite dans de nombreux pays. Les personnes engagées dans la recherche alchimique ont été accusées de sorcellerie et brûlées sur le bûcher.
1er CHIMISTE. Mais je peux facilement obtenir de l'or avec un simple clou de fer.
Expérience de démonstration
"Couteau d'or"
Préparez un couteau en fer ou un clou nettoyé avec du papier de verre. Plongez ce couteau ou ce clou dans une solution concentrée de sulfate de cuivre. Le couteau ou le clou devient "doré".
2ème CHIMISTE. Mais la science ne peut pas être interdite, alors les scientifiques ont supprimé le préfixe "al-" du mot "alchimie", et un nouveau nom a été obtenu - "chimie". C'est le nom donné à la science qui étudie les substances qui nous entourent, ainsi que leurs propriétés et leurs transformations.
3ème CHIMISTE. Si dans les temps anciens, les gens effectuaient des transformations, ils étaient alors considérés comme de grands magiciens. Et je ne suis pas un magicien, mais je peux facilement obtenir "l'élixir de vie", que les alchimistes n'ont jamais réussi à obtenir.
Expérience de démonstration
"Caméléon"
Verser une solution de chromate de potassium dans un verre en l'acidifiant avec quelques gouttes d'acide sulfurique. Tout en agitant la solution orange avec une tige de verre, versez la solution de peroxyde d'hydrogène : une coloration bleue apparaît, qui vire rapidement au vert.
4ème CHIMISTE. Aussi un miracle pour moi - un élixir. Regardez, je peux obtenir instantanément du vin ou du lait à partir de l'eau, et du vin, au contraire, je peux obtenir de l'eau.
Expérience de démonstration
"Obtenir du vin et du lait"
Obtention de vin par l'interaction de solutions de phénolphtaléine et d'alcali ; obtenir du lait par l'interaction de solutions d'acide sulfurique et de chlorure de baryum.
Expérience de démonstration
"Changement de solution cramoisie en incolore"
Verser une solution de KMnO 4 dans un verre, acidifier avec H 2 SO 4 (conc.), puis ajouter H 2 O 2 goutte à goutte à cette solution. La solution de framboise devient incolore.
1er CHIMISTE. En utilisant la substance la plus courante sur Terre, de nombreuses transformations différentes peuvent être effectuées. Quelle est la substance la plus courante sur Terre ? Oui. C'est de l'eau.
2ème CHIMISTE. Écoutez le poème sur l'eau :
"Comme habillé de dentelle
Arbres, buissons, fils.
Et cela ressemble à un conte de fées
En fait, ce n'est que de l'eau.
L'étendue infinie de l'océan
Et le marigot tranquille de l'étang,
La cascade de la cascade et le jet de la fontaine,
Et tout cela n'est que de l'eau.
Comment porter en hiver
Champs indigènes blancs comme neige,
Mais le temps viendra, tout fondra,
Et il y aura de l'eau claire.
La formule de cette substance étonnante est H 2 O. De nombreuses transformations intéressantes et amusantes peuvent être réalisées avec de l'eau.
Expérience de démonstration
"Interaction du potassium avec l'eau"
Ajouter 3 gouttes de solution de phénolphtaléine à un verre d'eau et ajouter un petit morceau de potassium métallique.
Expérience de démonstration
"liquide auto-inflammable"
Placez les cristaux de KMnO 4 broyés dans une tasse en porcelaine, puis ajoutez-y 3 à 4 gouttes de glycérine à l'aide d'une pipette. Au bout d'un moment, la glycérine s'enflamme et brûle.
Expérience de démonstration
"Flamme sur l'eau"
Dans une cuillère pour brûler des substances, chauffer la poudre de magnésium sur une flamme, puis plonger la cuillère dans un flacon avec de l'eau. Une réaction violente se produit avec la libération d'hydrogène gazeux, qui s'enflamme.
Expérience de démonstration
" Nuage de feu "
Fixez le tube à essai dans le porte-tube à essai et remplissez-le au 1/3 avec des morceaux de paraffine. Faire chauffer la paraffine à vive ébullition et la verser d'une hauteur de 10 cm en un mince filet dans un bocal d'eau. La paraffine s'enflamme, formant une grande flamme.
Expérience de démonstration
"6 verres"
Dans le premier verre - 100 ml d'eau, l'eau est versée dans le second verre contenant 2-3 cristaux de chlorure de fer (III), les cristaux se dissolvent. Cette solution est versée dans un troisième bécher contenant 1 ml de solution d'hexacyanoferrate(II) de potassium. Une couleur bleue apparaît en raison de la formation de bleu de Prusse. Versez la solution bleue dans le quatrième verre, où 3-4 granules d'hydroxyde de sodium sont placés. Dans ce cas, une coloration brune apparaît dans tout le volume, due à l'hydroxyde de fer(III). Le contenu du quatrième verre est versé dans le cinquième verre avec 5 gouttes de solution de phénolphtaléine. La solution prend une couleur violette. Ce liquide est versé dans le sixième verre, au fond duquel se trouvent 5 à 6 gouttes d'acide chlorhydrique concentré. À la suite d'une neutralisation alcaline avec un acide, la phénolphtaléine perd sa couleur, mais la couleur bleue du bleu de Prusse réapparaît.
Expérience de démonstration
"Esquimau"
Verser 30 g de saccharose dans un bécher et ajouter 12 ml de H 2 SO 4 (conc.). Le mélange bout, formant une masse poreuse.
3ème CHIMISTE. Avez-vous déjà vu de la neige brûlante ? Regardez ici.
Expérience de démonstration
"Neige brûlante"
Versez de la neige dans le pot et compactez-le. Faites ensuite un évidement dans celui-ci, où placer un morceau de carbure de calcium. Apportez-lui une allumette allumée. La neige (plus précisément, le gaz qui s'échappe) commence à brûler.
4ème CHIMISTE. Pourquoi pensez-vous que les substances peuvent brûler ? Dans quelles conditions les substances brûlent-elles ? (L'oxygène doit être disponible.) La réaction de combustion est une réaction très importante en chimie. Regardez ce qui peut arriver aux substances lorsqu'elles brûlent.
Expérience de démonstration
"Poudre brûlante"
Préparez la poudre à canon à l'avance : un mélange de 7 parties de nitrate de potassium, 1 partie de soufre et 1 partie de charbon. Mettez le mélange dans une lame et mettez le feu. La poudre à canon brûle rapidement avec un sifflement.
Expérience de démonstration
"Volcan"
Décomposition du bichromate d'ammonium auquel on peut ajouter de la poudre de magnésium. Dans ce cas, la poudre (NH 4) 2 Cr 2 O 7 est versée dans une tasse en porcelaine avec un cône et incendiée avec un éclat brûlant.
Expérience de démonstration
"Blizzard de feu"
Dans un ballon à fond rond, humidifier préalablement les parois avec de l'ammoniaque. Placez l'oxyde de chrome (III) dans une cuillère pour les substances brûlantes, chauffez-le et versez-le dans un flacon avec de l'ammoniac. Une gerbe d'étincelles se forme.
Expérience de démonstration
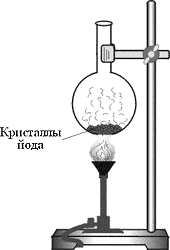 |
Mettre quelques cristaux d'iode dans un ballon à fond rond, chauffer le ballon sur une flamme de brûleur. L'iode est sublimé d'une vapeur violette.
1er CHIMISTE. Il s'avère que tout peut brûler, mais que tout ne peut pas brûler.
Expérience de démonstration
"Écharpe ignifuge"
Rincez le mouchoir à l'eau, puis pressez-le légèrement et imbibez-le bien d'alcool. Saisissez le mouchoir avec des pinces à creuset et mettez-y le feu. L'alcool flambe, mais le mouchoir ne brûle pas.
2ème CHIMISTE. Rappelez-vous, même Prométhée a souffert pour avoir apporté le feu aux gens. Là où il y a du feu, il y a toujours beaucoup de fumée. Vous avez probablement déjà entendu le proverbe « Il n'y a pas de fumée sans feu », et je peux prouver le contraire.
Expérience de démonstration
"Fumer sans feu"
Interaction de solutions concentrées d'acide chlorhydrique et d'ammoniac à travers l'espace aérien. Humidifiez deux tiges de verre avec ces solutions et rapprochez-les. De la fumée est générée.
3ème CHIMISTE. Oui, nous les chimistes sommes de vrais sorciers. Peut-être que certains d'entre vous consacreront toute leur vie à la chimie. Ou peut-être que quelqu'un sera un grand scientifique et proposera un médicament qui s'appellera vraiment «l'élixir de vie», puis il pourra facilement traiter les gens. Nous pouvons maintenant vous montrer comment opérer complètement sans douleur.
Expérience de démonstration
"Infliger une blessure et la guérir"
Humidifiez votre main avec une solution de chlorure de fer(III). Après cela, humidifiez le couteau avec une solution de thiocyanate de potassium et passez-le légèrement sur votre main. Une traînée rouge sang se forme.
4ème CHIMISTE. Et enfin, nous voulons vous surprendre avec cela. Regardez.
Expérience de démonstration
"Réception et explosion de gaz explosif"
Recueillir 2 petits volumes d'hydrogène et 1 volume d'oxygène en déplaçant de l'eau dans un bocal. Lorsque le bocal est plein, mettez le feu au mélange de gaz avec un éclat. Il y a une explosion assourdissante.
1er CHIMISTE. C'est là que votre voyage se termine. Vous avez tous fait face aux difficultés et n'avez pas eu peur du tout. Vous avez prouvé que vous pouviez devenir chimiste. Et ainsi j'ai eu l'honneur de vous initier aux chimistes.
Chaque élève reçoit un emblème et est félicité.
2ème CHIMISTE. Nous vous félicitons du fait qu'à partir d'aujourd'hui, vous pouvez vous considérer comme un vrai chimiste. Et nous voulons terminer notre soirée avec l'hymne des chimistes :
À bientôt!
E.V.KOZHURA,
professeur de chimie à l'école d'astronautique
(Jeleznogorsk, Territoire de Krasnoïarsk)
Ce n'est pas à propos phenomene naturel et non sur les étincelles d'un incendie. "Firestorm" est le nom d'une belle expérience de chimie. Pour le réaliser vous aurez besoin de :
- un récipient d'un volume supérieur à trois litres;
- cuillère brûlante;
- réchaud à alcool ou brûleur à gaz;
- conc. solution d'ammoniac (ou un mélange de sel d'ammonium et d'alcali solide);
Remplissez le récipient d'ammoniac de l'une des manières suivantes :
- versez-y 20 ml de solution concentrée d'ammoniac, couvrez de verre et attendez 10 minutes;
- versez un mélange de chlorure ou de nitrate d'ammonium et d'un alcali solide (par exemple, NaOH) dans le fond d'un récipient en verre, humidifiez-le avec de l'eau et laissez reposer un moment.
Ajoutez de l'oxyde de chrome (III) dans une cuillère brûlante à la flamme d'une lampe à alcool (brûleur). Dès que ses particules sont chauffées au rouge, versez la poudre d'oxyde dans un récipient avec de l'ammoniac. Là, les grains d'oxyde deviendront encore plus chauds et des étincelles de feu tomberont au fond.
Ce phénomène est basé sur le processus d'oxydation de l'ammoniac avec l'oxygène atmosphérique sous l'action d'un catalyseur - l'oxyde de chrome (III) :
Les « flocons de neige » brûlants sont des particules de catalyseur qui sont encore plus chauffées par la chaleur générée lors de la réaction.
Dès que la combustion s'arrêtera, le récipient sera rempli de gaz brun, et un peu plus tard - de fumée blanche. Leur origine est :

Nuage blanc dans une fiole
Avec l'ammoniac, vous pouvez réaliser d'autres belles expériences chimiques. Par exemple, dans n'importe quel film, qu'il s'agisse d'un conte de fées, d'une comédie ou de science-fiction, il y a dans le laboratoire de chimie des flacons dans lesquels tourbillonne de la fumée blanche. Obtenez-le à l'aide du même ammoniac.
Pour mener l'expérience, faites le plein d'un flacon et de réactifs :
- solution d'ammoniac à 10 % ;
- acide chlorhydrique concentré;
- carbonate de potassium solide.
 Versez du sel (K2CO3) dans le flacon et remplissez-le d'une solution d'ammoniac de manière à ce que la couche liquide au-dessus des cristaux ne dépasse pas 2 mm. Versez l'acide doucement sur le dessus. C'est alors que vous verrez un filet blanc de "fumée". Il va monter du fond du flacon et, sous son propre poids, se déposer le long des parois du vase.
Versez du sel (K2CO3) dans le flacon et remplissez-le d'une solution d'ammoniac de manière à ce que la couche liquide au-dessus des cristaux ne dépasse pas 2 mm. Versez l'acide doucement sur le dessus. C'est alors que vous verrez un filet blanc de "fumée". Il va monter du fond du flacon et, sous son propre poids, se déposer le long des parois du vase.
Ce phénomène non naturel s'explique simplement :
Le NH3 réagit avec l'acide chlorhydrique pour former une fumée blanche - des particules de chlorure d'ammonium en suspension dans l'air.
Le carbonate de potassium réagit avec le même acide pour former un autre sel (KCI) et un nouvel acide. Cependant, l'acide carbonique (H2CO3) est instable et se décompose immédiatement en dioxyde de carbone et en eau.
Le chlorure d'ammonium forme une suspension dans l'air et le dioxyde de carbone rapidement libéré l'entraîne. Comme le CO2 est plus lourd que l'air, le mélange gazeux descend lentement.

Comme vous pouvez le constater, même les expériences chimiques les plus mystérieuses et les plus belles sont un ou deux processus chimiques, de sorte que chaque chimiste, même débutant, peut les répéter. Surtout, n'oubliez pas de suivre les règles de sécurité lorsque vous travaillez dans un laboratoire de chimie. DANS Par ailleurs miracle se termine en tragédie.
Expérience chimique "Fire foam" - vidéo
tempête de feu
"Fiery blizzard" est l'une des plus belles expériences chimiques. Dans la forme "classique", cela ressemble à ceci. Une petite solution d'ammoniaque concentrée est versée dans un grand pot ou un flacon (vous pouvez également utiliser un mélange de sel d'ammonium et d'alcali, légèrement humidifié avec de l'eau). Le récipient est fermé et attend plusieurs minutes jusqu'à ce qu'il soit rempli de vapeur d'ammoniac (pour accélérer ce processus, le pot ou le flacon peut être légèrement tourné afin que la solution se répartisse sous forme de film sur sa partie inférieure). Après cela, le récipient est ouvert et une cuillerée d'oxyde de chrome (III) Cr 2 O 3 y est introduite, préchauffée dans une flamme de brûleur au feu rouge. Avec de légers mouvements de la cuillère, des particules d'oxyde de chrome sont pulvérisées.
Un véritable blizzard ardent commence dans le bocal: au lieu de se refroidir et de s'éteindre, les particules d'oxyde de chrome se réchauffent encore plus, le bocal est rempli d'étincelles rouges et jaunes, et ce n'est pas seulement une "pluie de feu", mais un " blizzard de feu » : les flux de gaz captent les particules incandescentes et les transportent dans différentes directions, y compris vers le haut et sur les côtés. De nombreux tourbillons enflammés sont observés, parfois une flamme jaune apparaît.
De nombreux lecteurs ont déjà compris que l'oxydation catalytique de l'ammoniac par l'oxygène atmosphérique se produit dans l'expérience à la surface des particules d'oxyde de chrome. Or, comme nous l'avons déjà vu, l'oxyde de chrome (III) est un catalyseur d'oxydation d'un grand nombre matière organique notamment les hydrocarbures. Il serait logique de tenter l'expérience "Fire Blizzard" avec un mélange propane-butane. Nous n'avons pas vu de description d'une telle expérience dans la littérature, mais, comme on dit : une tentative n'est pas une torture.
Un bocal de trois litres (que l'on appelle dans la vie de tous les jours une "bouteille de mise en conserve") était rempli d'un mélange propane-butane. Dans une cuillère improvisée, de l'oxyde de chrome (III), obtenu par décomposition de dichromate d'ammonium, a été chauffé. Lorsque l'oxyde de chrome était rouge par endroits, une cuillère a été introduite dans le pot avec le mélange et le contenu a commencé à être légèrement dispersé. En conséquence, des étincelles rouges et jaunes séparées sont apparues pour la première fois, puis une pluie ardente a commencé, qui s'est transformée en un blizzard ardent. L'expérience ressemblait à une expérience similaire avec de l'ammoniac, le blizzard était souvent encore plus brillant, mais une différence significative a également été observée: le mélange propane-butane s'est souvent enflammé, c'est-à-dire avec la combustion de surface, la combustion volumétrique a également commencé. Si la flamme était à l'intérieur du pot, cela n'a pas beaucoup gâché l'expérience (la flamme tourbillonnante avec des particules d'oxyde de chrome chaudes était également magnifique), mais lorsque la flamme s'est concentrée près du cou, le blizzard ardent s'est arrêté. Je devais également m'assurer que le mélange propane-butane dans la canette n'était pas accidentellement enflammé par un brûleur à proximité. Si cela s'est produit, le bocal aurait dû être rapidement recouvert d'un couvercle.
Au cours de l'expérience (surtout dans sa partie finale), la vie a été grandement compliquée par la vapeur d'eau, qui s'est condensée sur les parois de la jarre, ce qui a gêné l'observation (l'eau est un produit de l'oxydation des hydrocarbures). Lorsque l'expérience a été répétée dans le même bocal, ce problème a disparu : après plusieurs expériences, les parois du bocal ont été chauffées et l'eau a cessé de se condenser dessus. Il peut être conseillé de chauffer un peu le bidon avant de le remplir avec le mélange propane-butane (par exemple, dans une étuve ou un four).
La dernière partie de l'expérience (combustion catalytique) est mieux observée dans l'obscurité. Pour ce faire, il est souhaitable non seulement d'éteindre la lumière et d'assombrir la pièce, mais également d'éteindre le brûleur à gaz.
tempête de feu, le volcan de Böttger et le serpent de Pharaon sont obtenus auprès d'un expérimentateur curieux avec le kit d'expérimentation Tricks of Science.
L'ensemble Firestorm comprend :
- soucoupe en céramique
- dichromate d'ammonium
- glycérol
- permanganate de potassium (permanganate de potassium)
- urotropine
- gluconate de calcium
- ammoniac 10%
- Pipette Pasteur
- gants
- instruction
De plus, pour les expériences, vous aurez besoin d'une grande feuille de papier d'aluminium, d'un briquet pour cuisinières à gaz ou allumettes, bocal de 3 litres (non inclus dans le set).
Mieux vaut voir une fois qu'entendre cent fois
Veuillez lire la section Précautions de sécurité et suivre ses instructions avant de commencer à vous entraîner. Mettez des gants et recouvrez la table de papier d'aluminium. En connectant les composants sur le bol d'évaporation dans l'ordre spécifié, vous observez de véritables miracles de la science :
Volcan Bottger- l'expérience la plus brillante qui vous permet de recréer une "éruption" sûre avec la formation de cendres verdâtres. L'expérience porte le nom du scientifique qui a découvert le dichromate d'ammonium et a été la première personne au monde à observer cette réaction chimique spectaculaire.
serpent pharaon- une substance poreuse qui se tortille sur une soucoupe à la suite du mélange et de l'allumage de l'urotropine et du gluconate de calcium. Vous pouvez donner au "serpent" une forme intéressante avec un anneau en papier.
tempête de feu- l'expérience la plus spectaculaire, pour laquelle vous avez besoin d'un grand pot transparent. Après l'avoir rempli de vapeur d'ammoniaque et combiné les substances de la première expérience, on obtient un véritable ouragan d'étincelles jaunes et rouges derrière la vitre.
Pourquoi le kit est-il utile ?
Les connaissances acquises dans la pratique sont mieux assimilées. Ils seront utiles à l'enfant dans la poursuite de sa scolarité. L'observation des réactions chimiques vous permet d'élargir les idées des enfants sur le monde et de montrer à quel point les sciences naturelles sont intéressantes. L'ensemble présente le remarquable chimiste allemand qui a inventé les allumettes. Le spectacle des expériences est à couper le souffle.
À propos de la marque : Tricks of Science est une marque déposée d'Experimental Science. Elle est engagée dans le développement et la production de kits pour enfants pour de véritables expériences éducatives. Sa gamme est régulièrement renouvelée avec de nouvelles gammes de produits.
Créez une tempête de feu et d'autres merveilles avec le pack d'expérience Tricks of Science !
 budivel.ru A propos de l'isolation et du chauffage de la maison.
budivel.ru A propos de l'isolation et du chauffage de la maison.