इस नाम के तहत एक पाठ 7 वीं कक्षा में आयोजित किया जा सकता है। रसायन शास्त्र का अध्ययन करने से पहले, छात्रों को यह जानने में दिलचस्पी होगी कि रसायन शास्त्र क्या पढ़ रहा है, वे रसायन शास्त्र के पाठों में क्या करते हैं। पाठ हाई स्कूल के छात्रों (चार रसायनज्ञ छात्रों) द्वारा संचालित किया जाता है। समर्पण की शुरुआत से पहले, रसायन विज्ञान कक्ष को दीवार के समाचार पत्रों, नकली-अप और रासायनिक कांच के बने पदार्थ से सजाया जाता है। मनोरंजक प्रयोगों का प्रदर्शन किया जाता है, जो रसायन विज्ञान में रुचि के उद्भव में योगदान देता है।
लक्ष्य. चंचल तरीके से बच्चों को रसायन विज्ञान के बारे में, रासायनिक परिवर्तनों के बारे में, मानव जीवन में रसायन विज्ञान के महत्व के बारे में एक विचार दें।
कक्षाओं के दौरान
रसायनज्ञ (सभी एक साथ)। नमस्ते!
पहला रसायनज्ञ। हम रसायनज्ञ हैं! और केमिस्ट्री का मतलब है रातों की नींद हराम करना।
तीसरा रसायनज्ञ। ये रासायनिक प्रयोगशालाएं हैं।
चौथा रसायनज्ञ। ये माता-पिता हैं जो कहते हैं: "और हमारा बच्चा एक रसायनज्ञ है।"
सब। और वह जीवन है!
पहला रसायनज्ञ। लेकिन आप पूछ सकते हैं: हर कोई केमिस्ट क्यों नहीं बन जाता? हां, क्योंकि केमिस्ट्री रातों की नींद हराम है।
दूसरा रसायनज्ञ। यह एक सौ-यान-वें रसायन शास्त्र के बारे में बात है।
तीसरा रसायनज्ञ (नाक पकड़कर कहता है)। ये रासायनिक प्रयोगशालाएं हैं।
चौथा रसायनज्ञ। ये माता-पिता हैं जो कहते हैं: "और हमारा बच्चा (उह!) एक रसायनज्ञ है।"
सब। और वह जीवन है!
पहला रसायनज्ञ (गर्व से)। लेकिन फिर भी हम केमिस्ट हैं, क्योंकि केमिस्ट्री का मतलब है रातों की नींद हराम!
दूसरा रसायनज्ञ। यह रसायन विज्ञान के बारे में लगातार बात कर रहा है।
तीसरा रसायनज्ञ। ये हैं केमिस्ट्री लैब!
चौथा रसायनज्ञ। ये माता-पिता हैं जो कहते हैं: "और हमारा बच्चा (अपनी छाती पीटता है और गर्व से कहता है) एक रसायनज्ञ है!"
सब। और वह जीवन है!
पहला रसायनज्ञ। हमने कितनी किताबें और परियों की कहानियां पढ़ी हैं जिनमें अच्छी परी और शक्तिशाली जादूगर अद्भुत चमत्कार करते हैं!
दूसरा रसायनज्ञ। लेकिन फिर हमने कहानी को अंत तक पढ़ा, किताब को बंद कर दिया, और उसी क्षण, जैसे कि कोहरे में, जादूगर गायब हो गए, और चमत्कारों की केवल एक अस्पष्ट स्मृति बनी रही।
तीसरा रसायनज्ञ। हाँ, और कैसे? आखिरकार, जीवन में अभी तक कोई भी जादूगरों से नहीं मिला है, उनके साथ सड़कों पर चला गया, बात नहीं की।
चौथा रसायनज्ञ। लेकिन क्या इसका मतलब यह है कि जीवन में चमत्कार नहीं होते? किसी भी तरह से नहीं! लोग खुद चमत्कार करते हैं। लेकिन उन्हें इनकी इतनी आदत हो जाती है कि वे कुछ भी अद्भुत देखना बंद कर देते हैं। विज्ञान हमारे दिनों की सच्ची जादूगरनी है।
पहला रसायनज्ञ। और अगर हम चमत्कारों के बारे में बात करते हैं, तो अन्य सभी विज्ञानों में, रसायन विज्ञान विशेष रूप से बाहर खड़ा है। कोई आश्चर्य नहीं कि उसे एक अच्छी जादूगरनी कहा जाता है।
दूसरा रसायनज्ञ। यह एक व्यक्ति को अयस्कों और खनिजों से धातुओं को निकालने की अनुमति देता है, प्राकृतिक कच्चे माल से पदार्थ निकालने के लिए, दूसरे की तुलना में अधिक अद्भुत और अद्भुत। यह उपयोगी और महत्वपूर्ण गुणों के साथ सैकड़ों हजारों पदार्थों को जन्म देता है, जो प्रकृति में भी नहीं पाए जाते हैं।
तीसरा रसायनज्ञ। यह तेल को रबर और गैसोलीन में, गैस को कपड़े में, कोयले को इत्र, रंजक और औषधीय पदार्थों में बदल देता है। रसायन शास्त्र द्वारा किए गए अच्छे कर्मों की सूची वास्तव में अटूट है। रसायन हमें खिलाता है, कपड़े और जूते।
चौथा रसायनज्ञ। प्रत्येक व्यक्ति, इसे जाने बिना, घर से बाहर निकले बिना हर दिन रासायनिक प्रतिक्रियाएं करता है: अपने हाथों को साबुन से धोना, माचिस और गैस जलाना, भोजन बनाना। हाँ, और मानव शरीर अपने आप में एक बहुत बड़ा रासायनिक कारखाना है जिसमें कई रसायनिक प्रतिक्रिया.
पहला रसायनज्ञ।
खैर, बेशक, बिना किसी शक के,
केमिस्ट्री सीखनी होगी
सभी घटनाओं के ज्ञान के बिना
आज जीना असंभव है।
दूसरा रसायनज्ञ।
बेहतर करना होगा
हम, दोस्तों, शिक्षण में
और आपको आहें नहीं भरनी चाहिए
वह रसायन विज्ञान यातना है!
तीसरा रसायनज्ञ।
यदि आप रसायन शास्त्र नहीं जानते थे
हम हमेशा पैदल ही चलते थे:
ईंधन रहित बस
कभी नहीं जाएगा!
चौथा रसायनज्ञ।
हमारे लिए सामान्य रूप से बड़े होने के लिए
मजबूत और मजबूत
विटामिन रिलीज
साथ ही हमारी केमिस्ट्री!
पहला रसायनज्ञ।
ताकि पौधे बढ़े,
पदार्थों का अविष्कार हुआ है।
ऐसा हमारे लिए अच्छा होगा -
बड़े लोग जल्दी बड़े हो जाते हैं।
दूसरा रसायनज्ञ।
रबड़ प्रकृति में दुर्लभ है
आप इसके बिना नहीं रह सकते।
हम पोखरों से चलेंगे
महसूस किए गए जूतों में और बिना गला घोंटने के।
तीसरा रसायनज्ञ।
व्यापक रूप से हमारे जीवन में प्रवेश किया
विभिन्न प्लास्टिक।
बहुत ही कम समय में
जनता ने उन्हें स्वीकार कर लिया!
चौथा रसायनज्ञ।
बालों के लिए बहुलक दें
उत्तेजक विकास,
जल्दी से आविष्कार करें
फिर ब्रैड्स बढ़ेंगे।
पहला रसायनज्ञ। आज आपका रसायन विज्ञान से पहला परिचय है। हम आपको कुछ ऐसी तरकीबें दिखाएंगे जो आप जल्द ही एक रसायन विज्ञान के छात्र के रूप में करने में सक्षम होंगे।
डेमो अनुभव
"मार्टियन लैंडस्केप"
पोस्टर पर, फिनोलफथेलिन के अल्कोहल समाधान के साथ पहले से लिखें: "रसायन विज्ञान एक जादुई देश है," और फिर, प्रयोग दिखाते समय, रंगहीन शिलालेख को क्षार से सिक्त एक झाड़ू से पोंछ दें। शिलालेख बैंगनी हो जाएगा।
दूसरा रसायनज्ञ। हाँ, वास्तव में, रसायन विज्ञान एक जादुई भूमि है। आखिर ऐसा चमत्कार आपको और कहीं नहीं देखने को मिलेगा।
डेमो अनुभव
"बिना माचिस के आग जलाना"
प्रयोग के लिए केएमएनओ 4 और एच 2 एसओ 4 (सांद्र) का घोल तैयार करें। इस घोल में एक कांच की छड़ डुबोएं और इसे शराब में भीगी हुई रूई से स्पर्श करें। बड़ी मात्रा में गर्मी और ऑक्सीजन की रिहाई के साथ प्रतिक्रिया होती है:
3H 2 SO 4 (संक्षिप्त) + 2KMnO 4 \u003d K 2 SO 4 + 2MnSO 4 + 5 [O] + 3H 2 O।
शराब ज्वलनशील है।
तीसरा रसायनज्ञ। सदी के मध्य में ऐसे लोग थे जिन्होंने छोटी प्रयोगशालाओं में बहुत समय बिताया, अध्ययन किया विभिन्न पदार्थ. ये कीमियागर थे। कीमियागर ने धातुओं को सोने में बदलने की कोशिश की। राजाओं और राजाओं ने कीमियागर को अपने महलों में सोना लाने के लिए रखा।
चौथा रसायनज्ञ। लेकिन कीमियागर धातुओं को सोने में बदलने में विफल रहे, इसलिए कीमिया को कई देशों में प्रतिबंधित कर दिया गया था। जो लोग रसायन विज्ञान में लगे थे, उन पर जादू टोना का आरोप लगाया गया और उन्हें दांव पर लगा दिया गया।
पहला रसायनज्ञ। लेकिन मैं एक साधारण लोहे की कील से आसानी से सोना प्राप्त कर सकता हूं।
डेमो अनुभव
"सुनहरा चाकू"
एक लोहे का चाकू या कील तैयार करें जिसे सैंडपेपर से साफ किया गया हो। इस चाकू या कील को कॉपर सल्फेट के सांद्र विलयन में डुबोएं। चाकू या कील "सुनहरा" हो जाता है।
दूसरा रसायनज्ञ। लेकिन विज्ञान पर प्रतिबंध नहीं लगाया जा सकता है, इसलिए वैज्ञानिकों ने "कीमिया" शब्द से उपसर्ग "अल-" को हटा दिया, और एक नया नाम प्राप्त हुआ - "रसायन विज्ञान"। यह उस विज्ञान को दिया गया नाम है जो हमारे आस-पास के पदार्थों के साथ-साथ उनके गुणों और परिवर्तनों का अध्ययन करता है।
तीसरा रसायनज्ञ। यदि प्राचीन काल में लोग कुछ परिवर्तन करते थे, तो उन्हें महान जादूगर माना जाता था। और मैं कोई जादूगर नहीं हूं, लेकिन मुझे "जीवन का अमृत" आसानी से मिल सकता है, जिसे कीमियागर कभी हासिल नहीं कर पाए।
डेमो अनुभव
"गिरगिट"
एक गिलास में पोटेशियम क्रोमेट का घोल डालें, इसे सल्फ्यूरिक एसिड की कुछ बूंदों के साथ अम्लीकृत करें। नारंगी के घोल को कांच की छड़ से हिलाते समय, हाइड्रोजन पेरोक्साइड घोल डालें: एक नीला रंग दिखाई देता है, जो जल्द ही हरा हो जाता है।
चौथा रसायनज्ञ। मेरे लिए भी एक चमत्कार - एक अमृत। देखो, मैं जल से तुरन्त दाखमधु या दूध प्राप्त कर सकता हूं, और दाखरस से, इसके विपरीत, मुझे पानी मिल सकता है।
डेमो अनुभव
"शराब और दूध प्राप्त करना"
फिनोलफथेलिन और क्षार के विलयनों की परस्पर क्रिया द्वारा वाइन प्राप्त करना; सल्फ्यूरिक एसिड और बेरियम क्लोराइड के घोल की परस्पर क्रिया से दूध प्राप्त करना।
डेमो अनुभव
"रंगहीन करने के लिए क्रिमसन समाधान का परिवर्तन"
एक गिलास में KMnO 4 का घोल डालें, इसे H 2 SO 4 (सांद्र) से अम्लीकृत करें, फिर इस घोल में H 2 O 2 को बूंद-बूंद करके मिलाएं। रास्पबेरी का घोल रंगहीन हो जाता है।
पहला रसायनज्ञ। पृथ्वी पर सबसे आम पदार्थ का उपयोग करके, कई अलग-अलग परिवर्तन किए जा सकते हैं। आप क्या जानते हैं कि पृथ्वी पर सबसे आम पदार्थ क्या है? हां। यह पानी है।
दूसरा रसायनज्ञ। पानी के बारे में कविता सुनें:
"जैसे कि फीता में कपड़े पहने"
पेड़, झाड़ियाँ, तार।
और यह एक परी कथा की तरह लगता है
वास्तव में, यह सिर्फ पानी है।
सागर का असीम विस्तार
और तालाब का शांत बैकवाटर,
झरने का झरना और फव्वारे की फुहार,
और यह सब सिर्फ पानी है।
सर्दियों में कैसे पहनें
स्नो व्हाइट देशी खेत,
पर वक्त आएगा, सब पिघल जाएगा,
और सादा पानी होगा।
इस अद्भुत पदार्थ का सूत्र एच 2 ओ है। पानी के साथ कई रोचक और मनोरंजक परिवर्तन किए जा सकते हैं।
डेमो अनुभव
"पानी के साथ पोटेशियम की बातचीत"
एक गिलास पानी में फिनोलफथेलिन के घोल की 3 बूँदें डालें और धात्विक पोटेशियम का एक छोटा टुकड़ा डालें।
डेमो अनुभव
"स्व-प्रज्वलित तरल"
एक चीनी मिट्टी के बरतन कप में कुचले हुए KMnO 4 क्रिस्टल रखें, और फिर एक पिपेट से ग्लिसरीन की 3-4 बूंदें उनमें डालें। थोड़ी देर के बाद, ग्लिसरीन प्रज्वलित और जल जाता है।
डेमो अनुभव
"पानी पर लौ"
जलने वाले पदार्थों के लिए एक चम्मच में मैग्नीशियम पाउडर को आग पर गर्म करें, फिर चम्मच को पानी के साथ फ्लास्क में डुबो दें। हाइड्रोजन गैस की रिहाई के साथ एक हिंसक प्रतिक्रिया होती है, जो प्रज्वलित होती है।
डेमो अनुभव
"आग के बादल"
टेस्ट ट्यूब होल्डर में टेस्ट ट्यूब को ठीक करें और 1/3 को पैराफिन के टुकड़ों से भरें। पैराफिन को एक जोरदार उबाल में गरम करें और 10 सेमी की ऊंचाई से एक पतली धारा में पानी के जार में डालें। पैराफिन भड़क उठता है, जिससे एक बड़ी लौ बन जाती है।
डेमो अनुभव
"6 गिलास"
पहले गिलास में - 100 मिली पानी, दूसरे गिलास में लोहे (III) क्लोराइड के 2-3 क्रिस्टल युक्त पानी डाला जाता है, क्रिस्टल घुल जाते हैं। इस घोल को एक तीसरे बीकर में डाला जाता है जिसमें 1 मिली पोटैशियम हेक्सासायनोफेरेट (II) घोल होता है। प्रशिया नीला बनने के कारण नीला रंग दिखाई देता है। नीले घोल को चौथे गिलास में डालें, जहाँ सोडियम हाइड्रॉक्साइड के 3-4 दाने रखे हैं। इस मामले में, लोहे (III) हाइड्रॉक्साइड के कारण, पूरे आयतन में एक भूरा रंग होता है। चौथे गिलास की सामग्री को फिनोलफथेलिन समाधान की 5 बूंदों के साथ पांचवें गिलास में डाला जाता है। समाधान एक बैंगनी रंग लेता है। इस तरल को छठे गिलास में डाला जाता है, जिसके तल पर केंद्रित हाइड्रोक्लोरिक एसिड की 5-6 बूंदें होती हैं। अम्ल के साथ क्षार के उदासीनीकरण के परिणामस्वरूप, फिनोलफथेलिन अपना रंग खो देता है, लेकिन प्रशिया नीला का नीला रंग फिर से दिखाई देता है।
डेमो अनुभव
"एस्किमो"
एक बीकर में 30 ग्राम सुक्रोज डालें और एच 2 एसओ 4 (सांद्र) के 12 मिलीलीटर डालें। मिश्रण उबलता है, एक झरझरा द्रव्यमान बनाता है।
तीसरा रसायनज्ञ। क्या आपने कभी जलती हुई बर्फ देखी है? यहाँ देखो।
डेमो अनुभव
"जलती हुई बर्फ"
जार में बर्फ डालें और इसे कॉम्पैक्ट करें। फिर उसमें एक गड्ढा बना लें, जहां कैल्शियम कार्बाइड का टुकड़ा रख दें। उसके लिए एक जला हुआ माचिस लाओ। बर्फ (अधिक सटीक रूप से, बच निकलने वाली गैस) जलने लगती है।
चौथा रसायनज्ञ। आपको क्यों लगता है कि पदार्थ जल सकते हैं? पदार्थ किन परिस्थितियों में जलते हैं? (ऑक्सीजन उपलब्ध होना चाहिए।) रसायन शास्त्र में दहन प्रतिक्रिया एक बहुत ही महत्वपूर्ण प्रतिक्रिया है। देखें कि जलने पर पदार्थों का क्या हो सकता है।
डेमो अनुभव
"जलती बारूद"
बारूद पहले से तैयार करें: 7 भाग पोटेशियम नाइट्रेट, 1 भाग सल्फर और 1 भाग कोयले का मिश्रण। मिश्रण को एक स्लाइड में डालें और आग लगा दें। बारूद फुफकार से जल्दी जल जाता है।
डेमो अनुभव
"ज्वर भाता"
अमोनियम डाइक्रोमेट का अपघटन जिसमें मैग्नीशियम पाउडर मिलाया जा सकता है। इस मामले में, पाउडर (NH 4) 2 Cr 2 O 7 को एक चीनी मिट्टी के बरतन कप में एक शंकु के साथ डाला जाता है और एक जलती हुई छींटे से आग लगा दी जाती है।
डेमो अनुभव
"आग बर्फ़ीला तूफ़ान"
एक गोल तले वाले फ्लास्क में, दीवारों को पहले से अमोनिया से गीला कर लें। क्रोमियम (III) ऑक्साइड को एक चम्मच में जलने वाले पदार्थों के लिए रखें, इसे गर्म करें और इसे अमोनिया के साथ फ्लास्क में डालें। चिंगारी का ढेर बनता है।
डेमो अनुभव
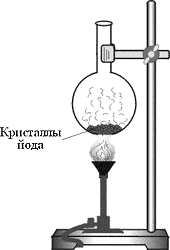 |
एक गोल नीचे वाले फ्लास्क में आयोडीन के कुछ क्रिस्टल रखें, फ्लास्क को बर्नर की लौ पर गर्म करें। आयोडीन एक बैंगनी वाष्प के साथ उच्चीकृत होता है।
पहला रसायनज्ञ। यह पता चला है कि सब कुछ जल सकता है, लेकिन सब कुछ नहीं जल सकता।
डेमो अनुभव
"अग्निरोधक दुपट्टा"
रूमाल को पानी में धो लें, फिर हल्का निचोड़ लें और शराब के साथ अच्छी तरह से भिगो दें। रुमाल को चिमटे से पकड़ें और आग लगा दें। शराब जलती है, लेकिन रूमाल नहीं जलता।
दूसरा रसायनज्ञ। याद रखें, यहां तक कि प्रोमेथियस को भी लोगों को आग लगाने के लिए नुकसान उठाना पड़ा था। जहां आग होती है, वहां हमेशा बहुत धुआं होता है। आपने शायद कहावत भी सुनी होगी "बिना आग के धुआँ नहीं होता", और मैं इसके विपरीत साबित कर सकता हूँ।
डेमो अनुभव
"आग के बिना धुआं"
वायु क्षेत्र के माध्यम से हाइड्रोक्लोरिक एसिड और अमोनिया के केंद्रित समाधानों की बातचीत। इन विलयनों से काँच की दो छड़ों को गीला करें और उन्हें एक साथ लाएं। धुआं उत्पन्न होता है।
तीसरा रसायनज्ञ। हाँ, हम केमिस्ट असली जादूगर हैं। हो सकता है कि आप में से कुछ लोग अपना पूरा जीवन रसायन शास्त्र के लिए समर्पित कर दें। या हो सकता है कि कोई एक महान वैज्ञानिक हो और एक ऐसी दवा लेकर आए जिसे वास्तव में "जीवन का अमृत" कहा जाएगा, और तब वह आसानी से लोगों का इलाज कर सकेगा। अब हम आपको दिखा सकते हैं कि बिना दर्द के पूरी तरह से कैसे काम करना है।
डेमो अनुभव
"एक घाव भरना और इसे ठीक करना"
अपने हाथ को आयरन (III) क्लोराइड के घोल से गीला करें। उसके बाद चाकू को पोटैशियम थायोसाइनेट के घोल से गीला कर लें और हल्के से अपने हाथ पर चला लें। एक रक्त लाल निशान बनता है।
चौथा रसायनज्ञ। और अंत में, हम आपको इससे आश्चर्यचकित करना चाहते हैं। घड़ी।
डेमो अनुभव
"विस्फोटक गैस की प्राप्ति और विस्फोट"
पानी को एक जार में रखकर 2 मात्रा में हाइड्रोजन और 1 मात्रा ऑक्सीजन एकत्र करें। जब जार भर जाता है, तो गैसों के मिश्रण को एक किरच से आग लगा दें। एक भयानक विस्फोट होता है।
पहला रसायनज्ञ। यहीं पर आपकी यात्रा समाप्त होती है। आप सभी ने कठिनाइयों का सामना किया और बिल्कुल भी नहीं डरे। आपने साबित कर दिया है कि आप केमिस्ट बन सकते हैं। और इसलिए मुझे आपको रसायनज्ञ के रूप में दीक्षा देने का सम्मान मिला।
प्रत्येक छात्र को एक प्रतीक दिया जाता है और बधाई दी जाती है।
दूसरा रसायनज्ञ। हम आपको इस बात के लिए बधाई देते हैं कि आज से आप खुद को एक असली केमिस्ट मान सकते हैं। और हम अपनी शाम को रसायनज्ञों के भजन के साथ समाप्त करना चाहते हैं:
जल्द ही फिर मिलेंगे!
ई.वी.कोजुरा,
एस्ट्रोनॉटिक्स स्कूल केमिस्ट्री टीचर
(ज़ेलेज़्नोगोर्स्क, क्रास्नोयार्स्क क्षेत्र)
यह इस बारे में नहीं है प्राकृतिक घटनाऔर आग की चिंगारियों के बारे में नहीं। "फायरस्टॉर्म" एक खूबसूरत रसायन विज्ञान के अनुभव का नाम है। इसे पूरा करने के लिए आपको आवश्यकता होगी:
- तीन लीटर से अधिक की मात्रा वाला एक बर्तन;
- जलती हुई चम्मच;
- स्पिरिट स्टोव या गैस बर्नर;
- संक्षिप्त अमोनिया समाधान (या अमोनियम नमक और ठोस क्षार का मिश्रण);
निम्नलिखित में से किसी एक तरीके से बर्तन को अमोनिया से भरें:
- इसमें 20 मिलीलीटर केंद्रित अमोनिया घोल डालें, ऊपर से कांच से ढक दें और 10 मिनट प्रतीक्षा करें;
- अमोनियम क्लोराइड या नाइट्रेट और एक ठोस क्षार (उदाहरण के लिए, NaOH) का मिश्रण एक कांच के कंटेनर के तल में डालें, इसे पानी से सिक्त करें और थोड़ी देर के लिए छोड़ दें।
एल्कोहल लैम्प (बर्नर) की लौ में एक जलते हुए चम्मच में क्रोमियम ऑक्साइड (III) मिलाएं। जैसे ही इसके कण लाल-गर्म गर्म होते हैं, ऑक्साइड पाउडर को अमोनिया वाले बर्तन में डालें। वहां ऑक्साइड के दाने और भी गर्म हो जाएंगे और आग की चिंगारियां नीचे तक गिरेंगी।
यह घटना उत्प्रेरक - क्रोमियम (III) ऑक्साइड की क्रिया के तहत वायुमंडलीय ऑक्सीजन के साथ अमोनिया के ऑक्सीकरण की प्रक्रिया पर आधारित है:
जलते हुए "स्नोफ्लेक्स" उत्प्रेरक कण होते हैं जो प्रतिक्रिया के दौरान उत्पन्न गर्मी से और भी अधिक गर्म होते हैं।
जैसे ही दहन बंद हो जाता है, बर्तन भूरे रंग की गैस से भर जाएगा, और थोड़ी देर बाद - सफेद धुएं से। उनका मूल है:

कुप्पी में सफेद बादल
अमोनिया के साथ, आप अन्य सुंदर प्रदर्शन कर सकते हैं रासायनिक प्रयोग. उदाहरण के लिए, किसी भी फिल्म में, चाहे वह परियों की कहानी हो, कॉमेडी हो या साइंस फिक्शन, एक रासायनिक प्रयोगशाला में फ्लास्क होते हैं जिसमें सफेद धुआं घूमता है। इसे उसी अमोनिया की मदद से लें।
प्रयोग करने के लिए, फ्लास्क और अभिकर्मकों पर स्टॉक करें:
- 10% अमोनिया समाधान;
- केंद्रित हाइड्रोक्लोरिक एसिड;
- ठोस पोटेशियम कार्बोनेट।
 फ्लास्क में नमक (K2CO3) डालें और इसे अमोनिया के घोल से भरें ताकि क्रिस्टल के ऊपर तरल परत 2 मिमी से अधिक न हो। ऊपर से धीरे से एसिड डालें। तभी आपको "धूम्रपान" की एक सफेद छल दिखाई देगी। यह फ्लास्क के नीचे से उठेगा और अपने वजन के नीचे बर्तन की दीवारों के साथ नीचे बैठ जाएगा।
फ्लास्क में नमक (K2CO3) डालें और इसे अमोनिया के घोल से भरें ताकि क्रिस्टल के ऊपर तरल परत 2 मिमी से अधिक न हो। ऊपर से धीरे से एसिड डालें। तभी आपको "धूम्रपान" की एक सफेद छल दिखाई देगी। यह फ्लास्क के नीचे से उठेगा और अपने वजन के नीचे बर्तन की दीवारों के साथ नीचे बैठ जाएगा।
इस अप्राकृतिक घटना को सरलता से समझाया गया है:
NH3 हाइड्रोक्लोरिक एसिड के साथ सफेद धुआं बनाने के लिए प्रतिक्रिया करता है - हवा में निलंबित अमोनियम क्लोराइड के कण।
पोटैशियम कार्बोनेट उसी अम्ल से क्रिया करके एक अन्य लवण (KCI) तथा एक नया अम्ल बनाता है। हालांकि, कार्बोनिक एसिड (H2CO3) अस्थिर है और तुरंत कार्बन डाइऑक्साइड और पानी में विघटित हो जाता है।
अमोनियम क्लोराइड हवा में एक निलंबन बनाता है, और तेजी से जारी कार्बन डाइऑक्साइड इसे साथ ले जाता है। चूंकि CO2 हवा से भारी है, इसलिए गैस का मिश्रण नीचे की ओर रेंगता है।

जैसा कि आप देख सकते हैं, यहां तक कि सबसे रहस्यमय और सुंदर रासायनिक प्रयोग भी एक या दो रासायनिक प्रक्रियाएं हैं, इसलिए हर रसायनज्ञ, यहां तक कि एक नौसिखिया भी उन्हें दोहरा सकता है। सबसे महत्वपूर्ण बात, रासायनिक प्रयोगशाला में काम करते समय सुरक्षा नियमों का पालन करना न भूलें। पर अन्यथात्रासदी में चमत्कार समाप्त होता है।
रासायनिक प्रयोग "फायर फोम" - वीडियो
आग बर्फ़ीला तूफ़ान
"उग्र बर्फ़ीला तूफ़ान" सबसे सुंदर रासायनिक प्रयोगों में से एक है। "क्लासिक" रूप में, यह इस तरह दिखता है। एक बड़े जार या फ्लास्क में थोड़ा सा केंद्रित अमोनिया घोल डाला जाता है (आप अमोनियम नमक और क्षार के मिश्रण का भी उपयोग कर सकते हैं, जिसे पानी से थोड़ा सिक्त किया जाता है)। बर्तन को बंद कर दिया जाता है और कई मिनट तक प्रतीक्षा की जाती है जब तक कि यह अमोनिया वाष्प से भर न जाए (इस प्रक्रिया को तेज करने के लिए, जार या फ्लास्क को थोड़ा घुमाया जा सकता है ताकि घोल को उसके निचले हिस्से पर फिल्म के रूप में वितरित किया जा सके)। उसके बाद, बर्तन को खोला जाता है और एक चम्मच क्रोमियम ऑक्साइड (III) Cr 2 O 3, बर्नर की लौ में लाल गर्मी के लिए पहले से गरम किया जाता है, इसमें डाला जाता है। चम्मच की हल्की गति से क्रोमियम ऑक्साइड के कणों का छिड़काव किया जाता है।
जार में एक वास्तविक उग्र बर्फ़ीला तूफ़ान शुरू होता है: क्रोमियम ऑक्साइड के कण ठंडा होने और बाहर जाने के बजाय और भी अधिक गर्म हो जाते हैं, जार लाल और पीले रंग की चिंगारियों से भर जाता है, और यह केवल "आग की बारिश" नहीं है, बल्कि एक " आग बर्फ़ीला तूफ़ान ”: गैस का प्रवाह लाल-गर्म कणों को उठाता है और उन्हें अलग-अलग दिशाओं में ले जाता है, जिसमें ऊपर और किनारे भी शामिल हैं। कई ज्वलंत भंवर देखे जाते हैं, कभी-कभी एक पीली लौ दिखाई देती है।
कई पाठक पहले ही समझ चुके हैं कि क्रोमियम ऑक्साइड कणों की सतह पर प्रयोग में वायुमंडलीय ऑक्सीजन द्वारा अमोनिया का उत्प्रेरक ऑक्सीकरण होता है। हालांकि, जैसा कि हम पहले ही देख चुके हैं, क्रोमियम (III) ऑक्साइड एक बड़ी संख्या के ऑक्सीकरण के लिए उत्प्रेरक है कार्बनिक पदार्थविशेष रूप से हाइड्रोकार्बन में। प्रोपेन-ब्यूटेन मिश्रण के साथ "फायर ब्लिज़ार्ड" प्रयोग का प्रयास करना तर्कसंगत होगा। हमने साहित्य में इस तरह के अनुभव का वर्णन नहीं देखा है, लेकिन, जैसा कि वे कहते हैं: एक प्रयास यातना नहीं है।
एक तीन-लीटर जार (जिसे रोजमर्रा की जिंदगी में "कैनिंग बोतल" कहा जाता है) प्रोपेन-ब्यूटेन मिश्रण से भरा हुआ था। एक तात्कालिक चम्मच में, अमोनियम डाइक्रोमेट के अपघटन द्वारा प्राप्त क्रोमियम (III) ऑक्साइड को गर्म किया गया था। जब क्रोमियम ऑक्साइड जगह-जगह लाल-गर्म हो गया, तो मिश्रण के साथ एक चम्मच जार में लाया गया और सामग्री थोड़ी बिखरी हुई होने लगी। नतीजतन, पहले अलग-अलग लाल और पीले रंग की चिंगारियां दिखाई दीं, फिर तेज बारिश शुरू हुई, जो तेज आंधी में बदल गई। प्रयोग अमोनिया के साथ एक समान प्रयोग जैसा दिखता था, बर्फ़ीला तूफ़ान अक्सर और भी तेज होता था, लेकिन एक महत्वपूर्ण अंतर भी देखा गया था: प्रोपेन-ब्यूटेन मिश्रण अक्सर भड़क जाता था, अर्थात। सतह के दहन के साथ, बड़ा दहन भी शुरू हुआ। अगर लौ जार के अंदर थी, तो यह अनुभव को ज्यादा खराब नहीं करती थी (गर्म क्रोमियम ऑक्साइड कणों के साथ घूमने वाली लौ भी सुंदर लगती थी), लेकिन जब लौ गर्दन के पास केंद्रित हो गई, तो तेज बर्फ़ीला तूफ़ान बंद हो गया। मुझे यह भी सुनिश्चित करना था कि कैन में प्रोपेन-ब्यूटेन मिश्रण गलती से पास के बर्नर द्वारा प्रज्वलित नहीं किया गया था। अगर ऐसा होता है, तो जार को जल्दी से ढक्कन से ढक देना चाहिए था।
प्रयोग के दौरान (विशेषकर इसके अंतिम भाग में), जल वाष्प द्वारा जीवन बहुत जटिल था, जो जार की दीवारों पर संघनित होता था, जो अवलोकन में हस्तक्षेप करता था (पानी हाइड्रोकार्बन के ऑक्सीकरण का एक उत्पाद है)। जब उसी जार में प्रयोग दोहराया गया, तो यह समस्या गायब हो गई: कई प्रयोगों के बाद, जार की दीवारों को गर्म किया गया, और पानी उन पर संघनित होना बंद हो गया। प्रोपेन-ब्यूटेन मिश्रण के साथ कैन भरने से पहले कैन को थोड़ा गर्म करने की सलाह दी जा सकती है (उदाहरण के लिए, सुखाने वाले कैबिनेट या ओवन में)।
प्रयोग का अंतिम भाग (उत्प्रेरक दहन) अंधेरे में सबसे अच्छा देखा जाता है। ऐसा करने के लिए, न केवल प्रकाश बंद करना और कमरे को अंधेरा करना, बल्कि गैस बर्नर को बंद करना भी वांछनीय है।
आग बर्फ़ीला तूफ़ान, बॉटगर के ज्वालामुखी और फिरौन के सर्प को ट्रिक्स ऑफ साइंस प्रयोग किट के साथ एक जिज्ञासु प्रयोगकर्ता से प्राप्त किया जाता है।
फायरस्टॉर्म सेट में शामिल हैं:
- चीनी मिट्टी की तश्तरी
- अमोनियम डाईक्रोमेट
- ग्लिसरॉल
- पोटेशियम परमैंगनेट (पोटेशियम परमैंगनेट)
- यूरोट्रोपिन
- कैल्शियम ग्लूकोनेट
- अमोनिया 10%
- पाश्चर पिपेट
- दस्ताने
- निर्देश
इसके अतिरिक्त, प्रयोगों के लिए आपको एल्यूमीनियम पन्नी की एक बड़ी शीट की आवश्यकता होगी, एक लाइटर गैस स्टोवया माचिस, 3-लीटर जार (सेट में शामिल नहीं)।
सौ बार सुनने से एक बार देखना बेहतर है
कृपया सुरक्षा सावधानियां अनुभाग पढ़ें और व्यायाम शुरू करने से पहले इसके निर्देशों का पालन करें। दस्ताने पहनें और टेबल को पन्नी से ढक दें। वाष्पीकरण कटोरे पर घटकों को निर्दिष्ट क्रम में जोड़कर, आप विज्ञान के वास्तविक चमत्कारों का निरीक्षण करते हैं:
बॉटगर ज्वालामुखी- सबसे उज्ज्वल अनुभव जो आपको हरे रंग की राख के गठन के साथ एक सुरक्षित "विस्फोट" को फिर से बनाने की अनुमति देता है। प्रयोग का नाम उस वैज्ञानिक के नाम पर रखा गया है जिसने अमोनियम डाइक्रोमेट की खोज की थी और वह इस शानदार रासायनिक प्रतिक्रिया को देखने वाले दुनिया के पहले व्यक्ति थे।
फिरौन सांप- एक झरझरा पदार्थ जो यूरोट्रोपिन और कैल्शियम ग्लूकोनेट को मिलाने और प्रज्वलित करने के परिणामस्वरूप तश्तरी पर झूलता है। आप पेपर रिंग के साथ "साँप" को एक दिलचस्प आकार दे सकते हैं।
आग बर्फ़ीला तूफ़ान- सबसे शानदार प्रयोग, जिसके लिए आपको एक बड़े पारदर्शी जार की जरूरत है। इसे अमोनिया वाष्प से भरने और पहले प्रयोग से पदार्थों को मिलाने के बाद, आपको कांच के पीछे पीले और लाल रंग की चिंगारी का एक वास्तविक तूफान मिलता है।
किट क्यों उपयोगी है?
अभ्यास में प्राप्त ज्ञान बेहतर अवशोषित होता है। वे आगे की स्कूली शिक्षा में बच्चे के लिए उपयोगी होंगे। रासायनिक प्रतिक्रियाओं का अवलोकन आपको दुनिया के बारे में बच्चों के विचारों का विस्तार करने और यह दिखाने की अनुमति देता है कि प्राकृतिक विज्ञान कितने दिलचस्प हैं। सेट उत्कृष्ट जर्मन रसायनज्ञ का परिचय देता है जिन्होंने मैचों का आविष्कार किया था। प्रयोगों का नजारा लुभावनी है।
ब्रांड के बारे में:ट्रिक्स ऑफ साइंस प्रायोगिक विज्ञान का ट्रेडमार्क है। यह वास्तव में शैक्षिक अनुभवों के लिए बच्चों की किट के विकास और उत्पादन में लगा हुआ है। इसकी रेंज नियमित रूप से नई उत्पाद लाइनों के साथ अपडेट की जाती है।
ट्रिक्स ऑफ साइंस एक्सपीरियंस पैक के साथ एक आग्नेयास्त्र और अन्य चमत्कार बनाएं!
 budivel.ru घर के इन्सुलेशन और हीटिंग के बारे में।
budivel.ru घर के इन्सुलेशन और हीटिंग के बारे में।